[지디넷코리아]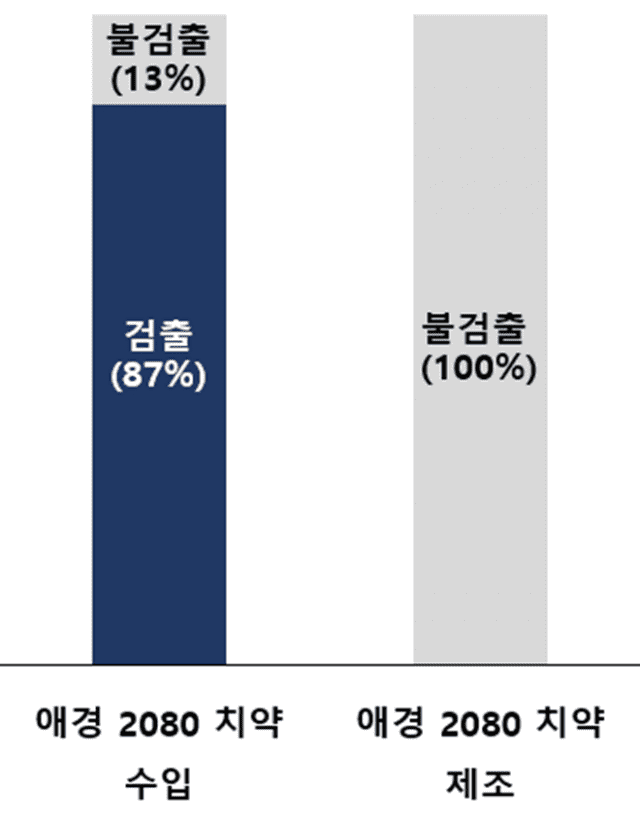
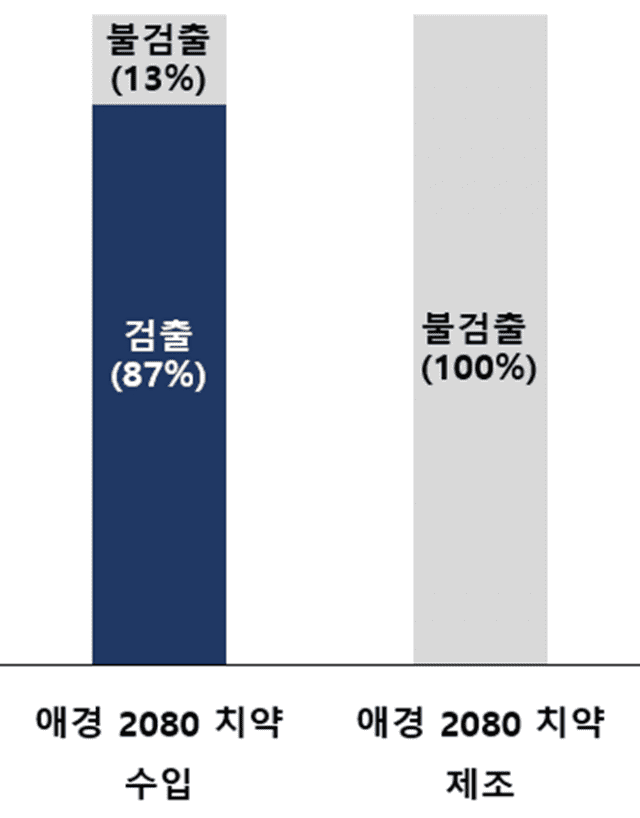
Domy에서 지난 2023년 2월부터 제조해 애경산업이 국내에 들여온 2080치약 수입제품 6종에서 트리클로산이 최대 0.16% 검출됐다. 국내 제조 제품에서는 해당 물질이 나오지 않았다.
트리클로산은 주로 치약 주성분, 세척·소독제, 보존제 용도로 쓰이는 성분이다. 2016년 이전에는 우리나라에서도 치약 제품에 0.3%까지 사용했던 성분이다. 식약처는 2016년부터 치약에서의 트리클로산 사용을 제한해 왔다.
국내 위해평가 전문가들은 트리클로산이 체내에서 빠르게 제거되어 축적 가능성이 적고, 인체 노출 위해평가 결과와 해외 기관들의 안전관리 기준 등을 고려할 때 0.3% 이하 트리클로산 함유 치약 사용에 대해 “위해 발생 우려는 낮은 수준”이라고 자문했다.

유럽 등지는 치약에 트리클로산이 0.3% 이하로 쓰이면 안전한 수준으로 평가한다.
식품의약품안전처의 해외제조소 조사 결과, 트리클로산이 수입 치약 제품에서 검출된 것은 Domy사가 2023년 4월부터 치약 제조 장비의 소독을 위해 트리클로산을 사용했던 것이 원인으로 밝혀졌다.
제조 장비에 잔류한 트리클로산 성분이 치약 제품에 섞였으며, 작업자별로 소독액 사용 여부와 사용량에 차이가 있어 치약 제품에 남은 잔류량이 일관되지 않게 나타났다.
또한 식약처는 트리클로산이 섞인 수입 치약을 국내에 유통한 애경산업에 대한 현장점검도 진행했다.

식약처에 따르면, 애경 측은 회수에 필요한 조치 지연 등 회수 절차를 준수하지 않았다. 의약외품 수입자는 안전성에 문제가 있는 사실 인지 시 바로 유통 중인 제품을 회수하거나 회수에 필요한 조치를 해야 한다. 5일 이내에 회수계획서를 제출해야 한다.
또 애경 측은 해외제조소에 대한 수입 품질관리가 미비한 점도 이번 식약처 조사에서 드러났다. 식약처는 애경산업에 대한 행정처분 절차를 진행할 예정이다.
앞으로 업체는 해외 치약을 최초 수입 시, 의무적으로 국내 판매 전 트리클로산 성적서를 식약처에 제출해야 한다. 판매 시, 매 제조번호별 트리클로산 자가품질검사도 의무화된다. 식약처는 제품 유통단계에서 수입 치약의 트리클로산 수거 및 검사를 확대하기로 했다.
이와 함께 치약 등 의약외품 해외제조소 점검 대상을 확대하고, 치약 중 위해 우려성분 모니터링 주기도 단축하기로 했다. 아울러 치약제 제조·품질관리 강화 등 위한 법령 개정도 추진할 예정이다.